
Las proteínas de membrana son proteínas asociadas o unidas a la membrana celular de los compartimentos celulares o de los orgánulos de una célula. Representan una de las clases de proteínas más grandes e importantes y pueden clasificarse como periféricas o integrales.
El Proteoma de Membrana
En las últimas décadas, el número de genes codificadores de proteínas humanas conocidos siempre ha variado ligeramente, pero en los últimos años el número absoluto gira en torno a los 20 000 genes (Piovesan, Antonaros y Vitale et al. 2019; Salzberg, 2018). Alrededor de un tercio de esas proteínas son proteínas secretadas o unidas a la membrana (consulte la Figura 1). Aunque se trata de una parte significativa de todo el proteoma, solo se conocen estructuralmente algunos de ellos. Dado que aproximadamente la mitad de todos los tratamientos aprobados se dirigen a las proteínas de membrana (consulte la Figura 2), la resolución de la estructura de estas proteínas de membrana terapéuticamente relevantes es muy favorable para el futuro diseño de fármacos (Baker, 2010).

¿Qué es una proteína de membrana?
El proteoma de membrana y el secretoma se cuentan como una de las clases de proteínas más grandes e importantes. Las proteínas de membrana se definen como proteínas asociadas o unidas a la membrana de una célula oa un orgánulo dentro de la célula. Se dividen en proteínas periféricas e integrales. Las proteínas de la membrana periférica se asocian temporalmente con la bicapa lipídica, pero no atraviesan completamente la membrana. La unión a la bicapa lipídica se logra mediante la perforación de regiones periféricas o mediante el acoplamiento con proteínas integrales de membrana (consulte la Figura 3, B y C). Estas proteínas integrales están incrustadas permanentemente, abarcan toda la bicapa lipídica y contienen estructuras hidrofóbicas de hélice alfa o barril beta que residen dentro de la membrana. Se pueden subdividir en grupos, como receptores o canales, según su función celular.
Junto con los dominios extracelulares e intracelulares hidrofílicos, la mayoría de las proteínas de membrana muestran un carácter anfipático. El carácter anfipático produce además una firma por la que a menudo se pueden identificar las proteínas integrales de la membrana. Esto se debe a que sus estructuras primarias contienen de 19 a 23 aminoácidos hidrofóbicos en sus secuencias lineales, necesarios para abarcar el interior hidrofóbico de una membrana. Los barriles β con residuos hidrófobos que apuntan hacia el exterior del barril también pueden actuar como un buen indicador de una proteína de membrana (Yeagle, 2016, The Membranes of Cells).

El papel crítico de las proteínas de membrana
En muchos procesos fisiológicos y patológicos, los reactivos, los factores de transcripción, las proteínas o los iones necesitan atravesar barreras de membrana. Si tienen éxito, desencadenan vías de señalización, envían factores de crecimiento y coagulación o transmiten señales de proteínas que no pueden cruzar la bicapa lipídica, como las citoquinas. Por lo tanto, las proteínas de membrana se ubican en una intersección muy importante de muchos procesos celulares.
Para ello, las proteínas de membrana asumen numerosas funciones críticas como el transporte de proteínas e iones a través de canales especiales o la transducción de señales dentro de muchos organismos. Son responsables de las uniones intercelulares o del reconocimiento célula-célula, lo que permite una comunicación rápida entre células y el reconocimiento efectivo de células extrañas, siendo de suma importancia para el sistema inmunitario.
Clasificación y Funciones de las proteínas de membrana
Clases
Actualmente, la TCDB (Base de datos de clasificación de transportadores) enumera 92 superfamilias con más de 1600 familias de transportadores en ellas. Debido a la gran cantidad de estos, solo nos gustaría presentar una pequeña descripción general de estas clases de transportadores a continuación:

1. ABC-Transportador
La superfamilia de transportadores de cassettes de unión a ATP es una de las familias de genes más grandes. En la mayoría de los casos, consisten en múltiples subunidades, divididas en dominios transmembrana hidrofóbicos y ATPasas hidrofílicas asociadas a la membrana. Al funcionar como bombas moleculares, utilizan la energía de la hidrólisis de ATP para mover varios solutos a través de las membranas celulares (Jones y George, 2002).
2. Canales Iónicos
Las proteínas formadoras de poros facilitan el flujo de iones a través de las membranas celulares. Se realiza una subdivisión según los tipos ya sea por clasificación en mecanismo de activación, por tipo de ion o por localización celular. Un tipo bien conocido del primer grupo son los canales iónicos activados por voltaje, como muchos canales de Na+, K+ o Ca2+. Biológicamente, son un componente clave del sistema nervioso. Asimismo, es igualmente importante su implicación en la contracción muscular o en la activación de las células T.
3. ATPasas unidas a membrana
Como su nombre lo indica, la superfamilia ATPasa utiliza ATP para realizar sus funciones. Se clasifican en ATPasas de tipo F, V y P. Las ATPasas de tipo F y V se clasifican como ATPasas rotativas, mientras que las ATPasas de tipo P impulsan sus cambios conformacionales utilizando la energía libre liberada por la hidrólisis de ATP (Palmgren y Nissen, 2011; Pizzagalli, Bensimon y Superti-Furga, 2020). Una ATPasa bien conocida es el intercambiador de Na+/K+, que bombea sodio y potasio en contra de sus gradientes de concentración para mantener el potencial de la membrana celular.
4. SLC-Transportador
Las proteínas transportadoras de solutos son una superfamilia de proteínas transportadoras que transfieren una amplia variedad de solutos a través de las membranas. Estos incluyen moléculas como azúcar, aminoácidos, vitaminas o metales (Hediger et al., 2013). Por tanto, actúan como uno de los principales reguladores de lo que entra o sale de una célula, y de ellos dependen muchos procesos tanto fisiológicos como celulares (Pizzagalli, Bensimon, y Superti-Furga, 2020).
5. Canales de agua
Las acuaporinas o canales de agua facilitan el flujo de agua a través de las membranas. Por lo tanto, juegan un papel elemental en el mantenimiento del balance hídrico.
Funciones
Pero no solo las clases de transportadores muestran una gran diversidad, sino que las funciones de las diferentes clases también son innegablemente complejas. Sin embargo, seis funciones principales primordiales son especialmente dignas de mención:
A. Actividad enzimática – procesión de metabolitos y sustratos para varias rutas metabólicas
B. Transducción de señales – los mensajeros químicos interactúan con los sitios de unión de proteínas de membrana para enviar señales.
C. Transporte (activo/pasivo) – mueve moléculas y otras sustancias a través de las diferentes membranas celulares
D. Reconocimiento célula-célula – identificación entre células, es decir, relevante para el sistema inmunitario
E. Uniones intercelulares – diferentes uniones, como uniones abiertas o uniones estrechas, conectan células vecinas
F. Anclaje/Adjunto – importante para la red del citoesqueleto, las ubicaciones de las proteínas y el mantenimiento de ciertas formas.


Composición, Estructura y Disposición
Las proteínas de membrana varían en su composición y disposición. Por lo tanto, diferentes proporciones de estructuras alfa-hélice o beta-barril implicarán diferentes disposiciones de esas proteínas. Estructuralmente, las proteínas de membrana a menudo son anfipáticas y tienen partes hidrofílicas e hidrofóbicas.
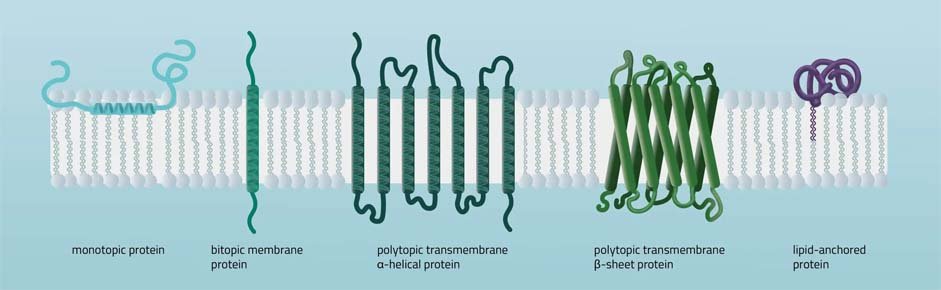
• Las proteínas integrales monotópicas están permanentemente unidas a un lado de la bicapa de la membrana. Los tipos de interacción implican, por ejemplo, una hélice α anfipática paralela al plano de la membrana (ver Figura 11) o varios bucles hidrofóbicos que anclan la proteína integralmente.
• Las proteínas integrales bitópicas atraviesan las bicapas lipídicas solo una vez. Una estructura bitópica típica consta del dominio transmembrana más los dos dominios celulares (extra e intra).
• Las proteínas transmembrana politópicas abarcan las bicapas lipídicas más de una vez. Son posibles diferentes composiciones de elementos alfa-helicoidales y beta-barriles en el dominio transmembrana (consulte la Figura 11 para ver dos ejemplos).
• Las proteínas ancladas en lípidos se unen covalentemente a los lípidos incrustados en la bicapa de fosfolípidos. Una interacción puede tener lugar por un enlace covalente con un lípido de membrana (lipidación) o por interacciones electrostáticas/iónicas con lípidos de membrana.
Como fue propuesto por primera vez en 1972 por Singer y Nicholson, la membrana celular consta de un mosaico de componentes, denominado modelo de mosaico fluido (Singer y Nicolson, 1972). Los fosfolípidos, el colesterol, las proteínas de membrana y los carbohidratos como componentes principales dan a las membranas su carácter fluido. Las proteínas integrales solo se unen de forma laxa a su entorno, lo que permite un ligero movimiento dentro de la membrana.
Tipos de procesos de transporte de membrana
En las membranas celulares, diferentes tipos de canales, transportadores y bombas permiten el transporte de sustancias a través de la bicapa lipídica. Muchos de ellos están altamente especializados para socios de interacción específicos y solo permiten ciertos transportes. En general, puede dividir los procesos de transporte en tres categorías más amplias: difusión, transporte pasivo y transporte activo.

Difusión simple
Movimiento de, ejemp. una molécula, ion o partícula de una región de mayor concentración, siguiendo su gradiente, a una región de menor concentración. El movimiento continúa hasta que se alcanza un equilibrio. Las partículas cargadas pueden cambiar este potencial de membrana en una dirección u otra.
Transporte pasivo
Analogon de la difusión simple para moléculas más grandes, como azúcares o aminoácidos. Las proteínas de transporte de membrana permiten el movimiento hacia abajo de un gradiente de concentración para sustratos que, en condiciones normales, no pueden atravesar la membrana.
• Proteínas de canal
Proteínas transmembrana especializadas que atraviesan la membrana celular. El mecanismo de activación puede desencadenarse por ligandos, cambios en el potencial de membrana o por procesos mecánicos (por ejemplo, cambios en el citoesqueleto).
• Proteínas transportadoras
Para este tipo de transporte pasivo, la molécula se transfiere a través de cambios conformacionales de un transportador especializado. El cambio se desencadena cuando un sustrato se acopla al transportador. Un medio de transporte puede tener lugar con una sola molécula (Uniport), con dos moléculas moviéndose en la misma dirección (Symport) o en direcciones opuestas (Antiport).
Transporte activo
El transporte activo es una forma de transporte que requiere energía del exterior para realizar su mecanismo. Esto permite el transporte de moléculas o iones contra sus gradientes de concentración o contra gradientes de potencial eléctrico. Las formas de energía pueden ser de naturaleza química (ATP) o de carga eléctrica. También es posible utilizar un gradiente de concentración como fuente de energía.
• Transporte activo primario
Los protones y los iones inorgánicos se mueven a través de la membrana celular aprovechando la energía del ATP. La bomba de Na-K es un ejemplo de esta forma de transporte, que transfiere tres iones de sodio cargados positivamente y dos iones de potasio igualmente cargados positivamente.
• Transporte activo secundario
De manera análoga a los simportadores y antiportadores de la proteína transportadora pasiva, esta vez uno de los iones se mueve con su gradiente de concentración mientras que el segundo se mueve contra él. Esto se puede lograr en la misma dirección (Symport) o en direcciones opuestas (Antiport). Por lo tanto, un gradiente electroquímico es una fuerza impulsora aquí.
• Transporte activo terciario
Para este tipo, tres transportadores deben funcionar en serie. Un primer transportador establece un gradiente electroquímico para la molécula A (activo primario). El segundo transportador utiliza la molécula A para establecer un gradiente electroquímico favorable para la molécula B (activo secundario). Finalmente, el transportador tres usa el gradiente de la molécula B para mover la molécula C contra su gradiente de concentración (Hamm, Alpern y Preisig, 2008).
• Translocación de grupo
Esta es una forma especial de transporte de bacterias. El sustrato a transportar se altera químicamente en el proceso. Como resultado, no se crea un gradiente de concentración. Como forma de energía, se puede utilizar ATP, pero existen otras fuentes de energía como PEP (sistema de fosfotransferasa), que también se utilizan para los procesos de transporte de glucosa (consulte la Figura 12, translocación de grupo).
Relevancia Histórica
Han pasado poco más de 50 años desde los comienzos de la biología molecular moderna de membranas en las décadas de 1960 y 1970. Descubrimientos como el desciframiento de la estructura molecular de la membrana celular o sus mecanismos generales subyacentes han allanado el camino para muchos conocimientos y campos de aplicación importantes en la medicina moderna. Mientras tanto, la caracterización de las proteínas unidas a la membrana enfrentó obstáculos aún mayores. Por lo tanto, tomó hasta 1978, cinco años después de la postulación del modelo de mosaico fluido, para reportar la primera caracterización exitosa de una proteína de membrana integral. Esta era glicoforina humana obtenida de la membrana celular de los eritrocitos (Singer, 2004).
Desde aquellos primeros días de la investigación de proteínas de membrana, se han logrado muchos hitos. En medicina, en particular, el conocimiento adquirido se ha utilizado en una variedad de formas para mejorar y combatir numerosas condiciones clínicas.
Retos y Perspectivas de Futuro para la Medicina / Industria

Fig. 13: Sistema de nanodiscos que rodea una proteína recortada
Las membranas celulares actúan como guardianes finales de muchos sustratos y fármacos. Las proteínas de membrana altamente especializadas, por lo tanto, interactúan en una fracción de segundo con una plétora de sustancias para determinar cuáles de ellas pueden pasar y cuáles no. Aproximadamente la mitad de todos los fármacos actualmente aprobados actúan sobre este tipo de proteína como una estructura diana terapéutica para causar transducciones de señales, desencadenar cascadas o catalizar reacciones para combatir diversas condiciones clínicas (Baker, 2010).
A pesar de esto, todavía se sabe poco sobre muchas estructuras de proteínas de membrana y sus principios de trabajo subyacentes, debido a sus desafiantes criterios de solubilización. La medicina moderna se beneficiaría enormemente de una comprensión más profunda de este tipo de proteína. Sin embargo, recientemente, este viejo problema está cobrando velocidad nuevamente, ya que varios sistemas de inteligencia artificial como AlphaFold2 de DeepMind se unen a la lucha. Son capaces de predecir una estructura de proteína 3D directamente a partir de su secuencia de aminoácidos con una precisión cada vez mayor.
Mientras tanto, los métodos experimentales que ya se están aplicando, como los sistemas de nanodiscos, los anfipollos modificados con cicloalcanos o los copolímeros AASTY, también seguirán desarrollándose, ampliando los límites de nuestro conocimiento.
En el futuro, el entrelazamiento de la IA y métodos experimentales como estos introducirá una nueva era de investigación biológica y médica, dando forma a campos como la biología digital o la computación biomédica. Los enfoques novedosos renovarán nuestros procesos de descubrimiento de fármacos, acelerándolos enormemente. Sea cual sea el camino que sigamos, el proteoma de membrana jugará un papel vital en él.
Literatura
Copyright © 2023 CIDSA Mexico. All rights reserved
Diseñado por Suguza Publicidad
