Este kit de ensayo Screen Quest™ proporciona un método simple y sensible para la medición de la captación de ácidos grasos en células que contienen transportadores de ácidos grasos.
Descripción
Kit de análisis de captación de ácidos grasos fluorimétricos Screen Quest™
La captación de ácidos grasos es un objetivo terapéutico importante para el tratamiento de muchas enfermedades humanas como la obesidad, la diabetes tipo 2 y la esteatosis hepática.
El kit de ensayo fluorométrico de captación de ácidos grasos Screen Quest™ proporciona un método simple y sensible para la medición de la captación de ácidos grasos en células que contienen transportadores de ácidos grasos. El kit utiliza un sustrato de ácido graso fluorescente de ácido dodecanoico patentado.
Este kit de ensayo de captación de ácidos grasos se puede realizar en cualquier lector de microplacas de fluorescencia con un modo de lectura inferior o canal FITC. El ensayo se puede realizar en placas de microtitulación de 96 pozos o de 384 pozos en un procedimiento simple de mezcla y lectura, y se puede adaptar fácilmente para aplicaciones que requieren alto volumen de detección. Kit para 100 pruebas.
Nombre en ingles: Screen Quest™ Fluorimetric Fatty Acid Uptake Assay Kit
| Catalogo | Producto | Presentación |
|---|---|---|
| 36385 | Kit de análisis de captación de ácidos grasos fluorimétricos Screen Quest™ | 100 pruebas |
Importante: Solo para uso en investigación (RUO).
Plataforma
Lector de microplacas de Fluorescencia
| Excitación | 485 nm |
| Emisión | 515 nm |
| Cutoff | 495 nm |
| Placa recomendada | Pared negra / fondo claro |
| Especificacion instrumento | Modo de lectura inferior |
Componentes
| Componente A: TF2-C12 Fatty Acid | 1 vial (liofilizado) |
| Componente B: Buffer de ensayo | 1 botella (10 mL) |
| Componente C: DMSO | 1 vial (100 µL) |
PREPARACION DE SOLUCION DE STOCK
A menos que se indique lo contrario, todas las soluciones madre no utilizadas deben dividirse en alícuotas de un solo uso y almacenarse a -20 °C después de la preparación. Evite los ciclos repetidos de congelación y descongelación.
Solución madre de ácidos grasos TF2-C12:
Agregue 20 µL de DMSO (Componente C) al vial de Ácido graso TF2-C12 (Componente A) y mezcle bien. Nota: 20 μL de la solución madre de sustrato de ácido graso fluorescente es suficiente para una placa. La solución madre de sustrato de ácido graso fluorescente no utilizada se puede dividir en alícuotas y almacenar a < -20 oC durante un máximo de dos meses si los tubos se sellan herméticamente y se mantienen alejados de la luz. Evite los ciclos repetidos de congelación y descongelación.
PREPARACION DE SOLUCION DE TRABAJO
Solución de carga de colorantes de ácidos grasos:
Agregue 20 µl de la solución madre de ácidos grasos TF2-C12 a 10 ml de buffer de ensayo (componente B) y mézclelos bien. Nota: 10 ml de solución de carga de colorante de ácidos grasos es suficiente para una placa; prepárelo fresco para cada experimento.
Imagenes

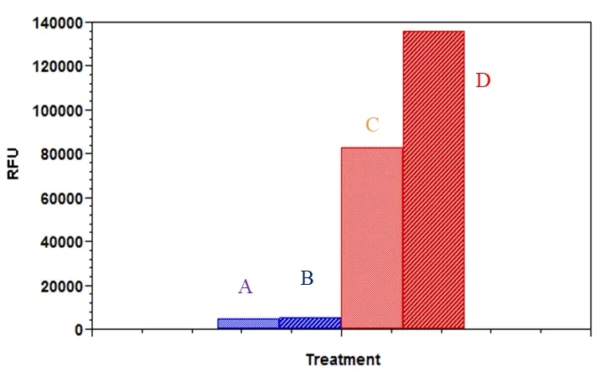
Figura 1. Comparación de la captación de ácidos grasos por adipocitos 3T3-L1 y fibroblastos. Las células se sembraron 50.000 células/100 ml/pozo en placa de 96 pozos con poli-D lisina de fondo transparente/pared negra durante 5 horas, y luego se privaron de suero durante 1 hora. Las células se trataron sin (control) o con insulina (150 nM), y se incubaron a 37 ºC, con CO2 al 5 % durante 30 min. Al final del tiempo de incubación, se añadieron 100 µl de mezcla de ácidos grasos al pozo y se incubó durante otros 60 min. La señal de fluorescencia se midió con un lector de placas FlexStation utilizando el modo de lectura inferior. A – fibroblastos (Control); B – fibroblastos (Insulina); C – adipocitos (Control); D– adipocitos (Insulina).
Productos relacionados
Bibliografía
Chemically synthesized osteocalcin alleviates NAFLD via the AMPK-FOXO1/BCL6-CD36 pathway
Authors: Zhang, Miao and Dong, Keting and Du, Qian and Xu, Jiaojiao and Bai, Xue and Chen, Lei and Yang, Jianhong
Journal: Journal of Translational Medicine (2024): 1–20
Insulin-stimulated translocation of the fatty acid transporter CD36 to the plasma membrane is mediated by the small GTPase Rac1 in adipocytes
Authors: Chan, Man Piu and Takenaka, Nobuyuki and Abe, Yuki and Satoh, Takaya
Journal: Cellular Signalling (2024): 111102
Mouse Memory CD8 T Cell Subsets Defined by Tissue-Resident Memory Integrin Expression Exhibit Distinct Metabolic Profiles
Authors: Sportiello, Mike and Poindexter, Alexis and Reilly, Emma C and Geber, Adam and Lambert Emo, Kris and Jones, Taylor N and Topham, David J
Journal: ImmunoHorizons (2023): 652–669
PRP19 Enhances Esophageal Squamous Cell Carcinoma Progression by Reprogramming SREBF1-Dependent Fatty Acid Metabolism
Authors: Zhang, Guang-Cong and Yu, Xiang-Nan and Guo, Hong-Ying and Sun, Jia-Lei and Liu, Zhi-Yong and Zhu, Ji-Min and Liu, Tao-Tao and Dong, Ling and Shen, Xi-Zhong and Yin, Jie
Journal: Cancer Research (2023): OF1–OF17
Andrographolide ameliorates hepatic steatosis by suppressing FATP2-mediated fatty acid uptake in mice with nonalcoholic fatty liver disease
Authors: Ran, Li-Sha and Wu, Ya-Zeng and Gan, Yi-Wen and Wang, Hong-Lian and Wu, Li-Juan and Zheng, Chun-Mei and Ming, Yao and Xiong, Ran and Li, Yong-Lin and Lei, Shi-Hang and others,
Journal: Journal of Natural Medicines (2022): 1–14
Referencias
Ver todas las 69 referencias: Citation Explorer
Significance of short chain fatty acid transport by members of the monocarboxylate transporter family (MCT)
Authors: Moschen I, Broer A, Galic S, Lang F, Broer S.
Journal: Neurochem Res (2012): 2562
Improved working memory but no effect on striatal vesicular monoamine transporter type 2 after omega-3 polyunsaturated fatty acid supplementation
Authors: Narendran R, Frankle WG, Mason NS, Muldoon MF, Moghaddam B.
Journal: PLoS One (2012): e46832
Munc18c provides stimulus-selective regulation of GLUT4 but not fatty acid transporter trafficking in skeletal muscle
Authors: Jain SS, Snook LA, Glatz JF, Luiken JJ, Holloway GP, Thurmond DC, Bonen A.
Journal: FEBS Lett (2012): 2428
Emerging risk factors for postpartum depression: serotonin transporter genotype and omega-3 fatty acid status
Authors: Shapiro GD, Fraser WD, Seguin JR.
Journal: Can J Psychiatry (2012): 704
Poultry fat decreased fatty acid transporter protein mRNA expression and affected fatty acid composition in chickens
Authors: Yuan J, Zhang B, Guo Y.
Journal: J Anim Sci Biotechnol (2012): 17